細胞未病エンジニアリング研究グループ
研究概要
身体機能と心の健康を総合的に向上させるための研究として、老化とそれに伴うサルコペニアを改善する機能性成分の探索・作用機序の解明、睡眠障害やうつ病などの精神・神経疾患の早期発見に資するバイオマーカーの探索を行っています。多サンプル対応した細胞モデルから個体機能評価が可能な動物モデルを組み合わせた一気通貫の体制で産学官連携を担い、超高齢化社会を迎えた本邦における健康寿命の延伸に貢献します。
研究課題
研究課題1:老化に伴う神経機能異常の予防・先制に向けた制御因子探索とその評価技術の開発
研究担当者:新海 陽一
老化はALSやアルツハイマー病など様々な神経疾患のリスク因子です。近年、この老化に伴う神経疾患の根本治療や早期診断を目指して、液-液相分離の制御法および可視化法の開発が期待されています。私は寿命の短い線虫C. elegansを用いて液-液相分離・神経機能・老化の制御因子群を明らかにし、その知見を利用したヒト細胞ハイスループット評価系を開発しています。また、これらの評価系を活用した疾患予防・先制に資する機能性物質の探索を進めています。
研究課題2:心と身体の健康寿命の延伸を目指した非侵襲未病マーカーの開発と時間栄養学の活用
研究担当者:大石 勝隆
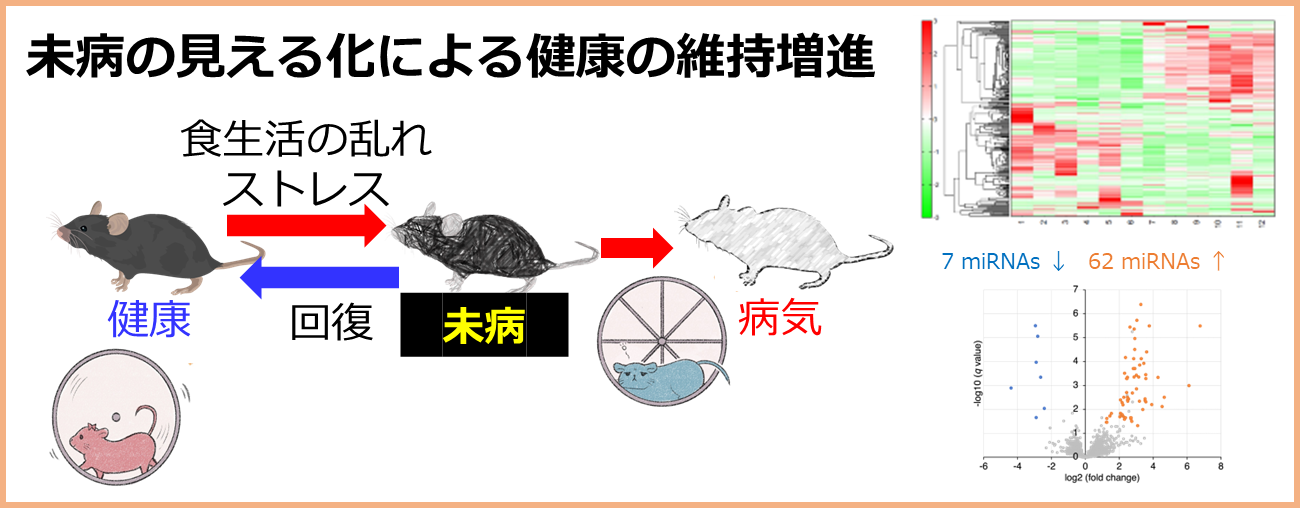
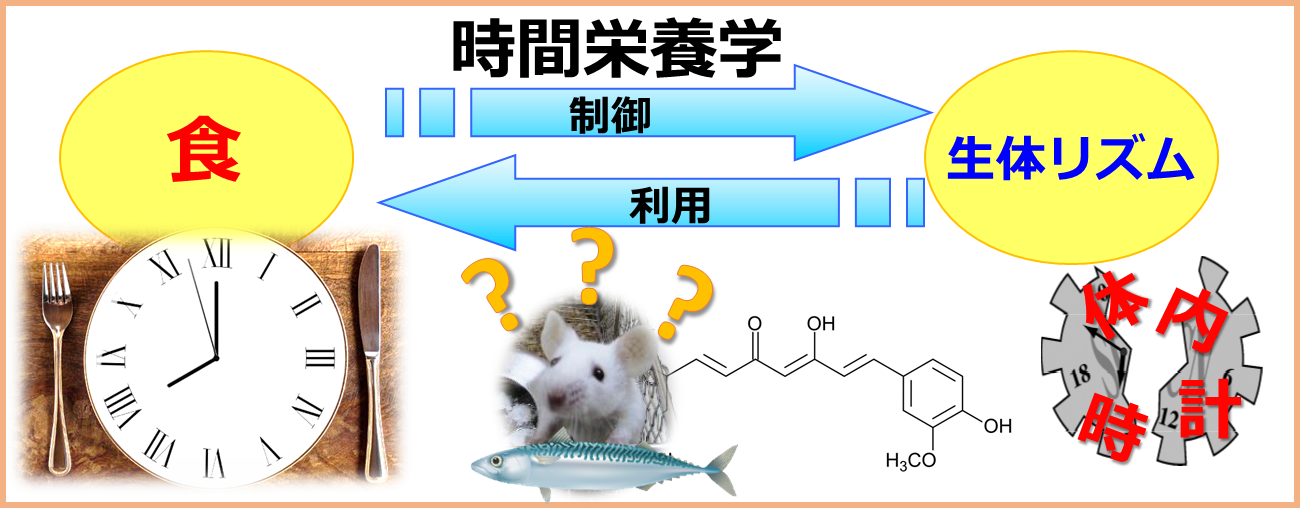
高齢者が生き生きと暮らせる社会の実現のためには、身体機能のみならず心の健康寿命の延伸が重要です。睡眠障害は、うつ病などの精神疾患や、高血圧や糖尿病といった生活習慣病の発症リスクを高めることが知られています。私たちは、疾患の発症につながるような慢性的な睡眠の乱れを、AI技術も活用しながら、非侵襲的に早期発見するためのバイオマーカーの開発を行っています。同時に、産学官の連携を積極的に推進することにより、時間栄養学を活用した睡眠や体内時計の積極的な制御技術の開発を行っています。
研究課題3:うつ病進行時に変化する疾患関連遺伝子と他疾患との相関機序
研究担当者:桑原 知子
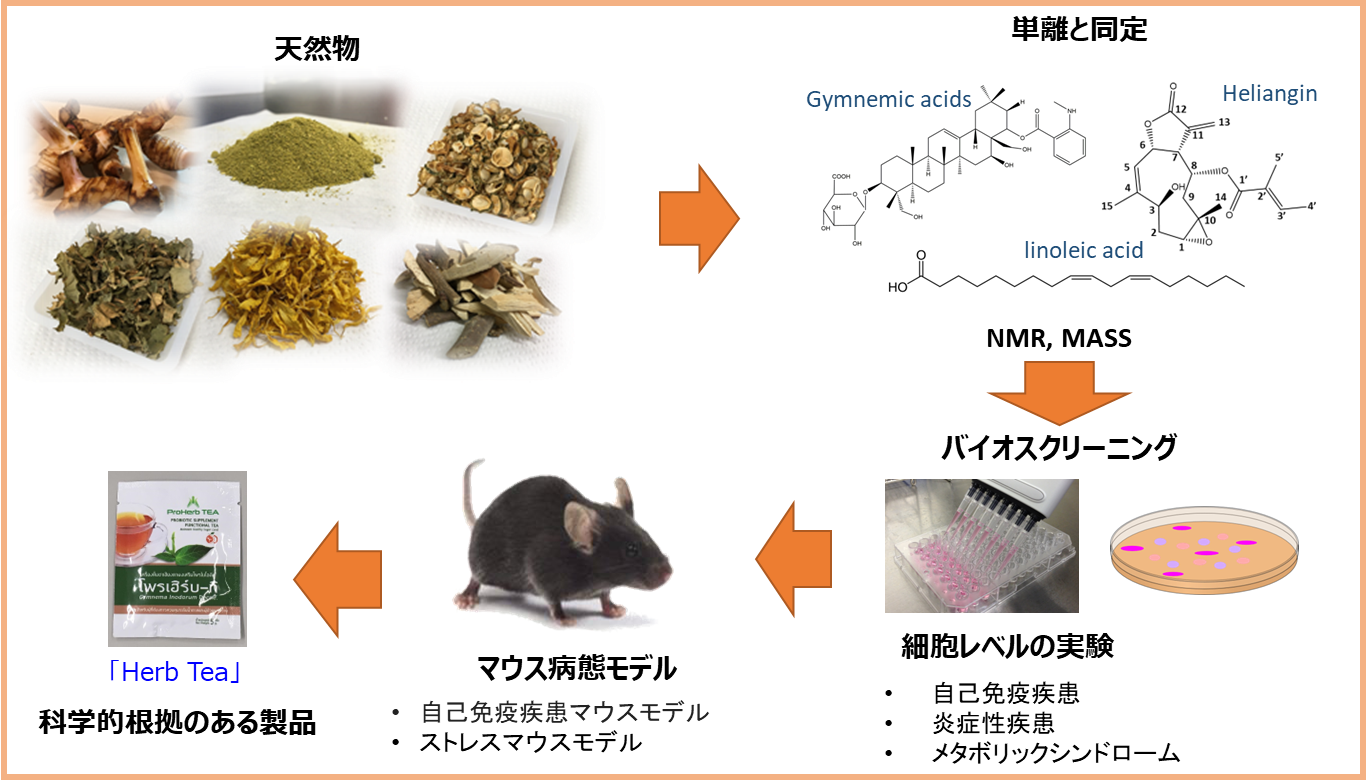
うつ病は罹患人口の増大化、標的患者層の広範化など大きな焦点をもちます。治療には必ず再発のリスクが伴う医学背景があります。他疾患に罹患している際に、潜在的にうつ病が進行加速する機序や、うつ病が原因で他疾患を誘引する背景の解明を目指しています。うつ病に関連して罹患リスクが増加する疾患、糖尿病や筋疾患など潜在的にうつ病発症増加リスクをもつ疾患などのモデル動物や、抽出し樹立した細胞培養系、誘導培養系らを比較解析します。各疾患のタイムコースに沿う候補遺伝子や作用因子、変化する細胞、臓器内領域を特定します。
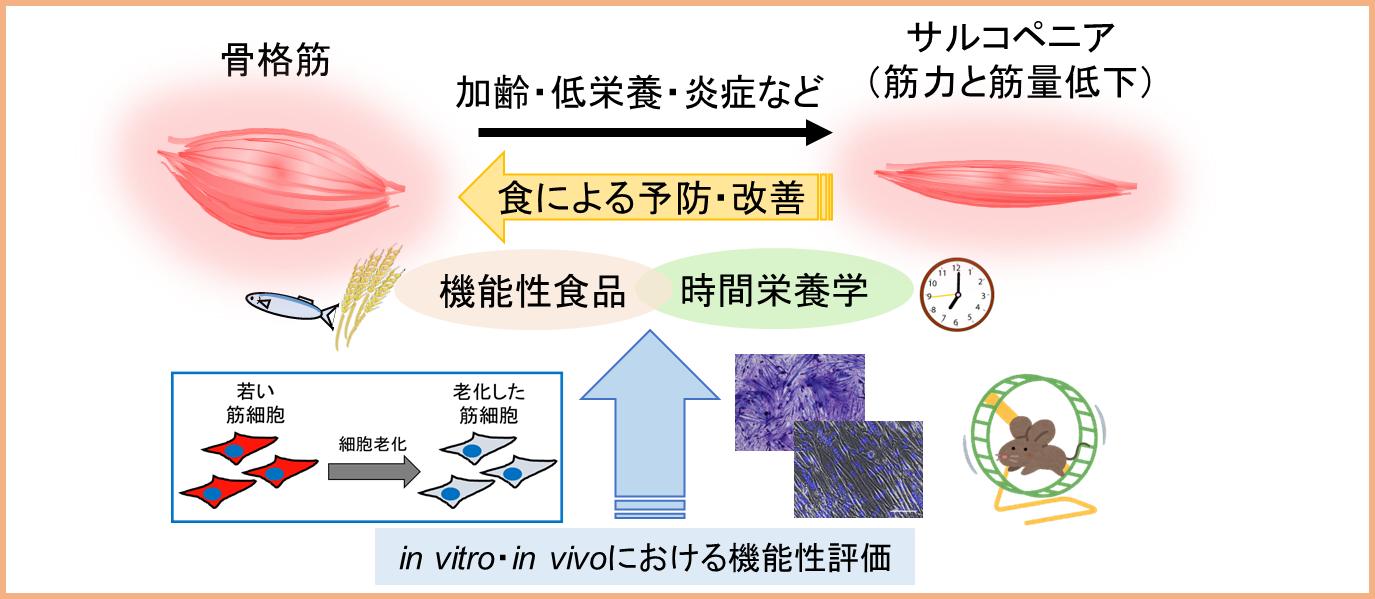
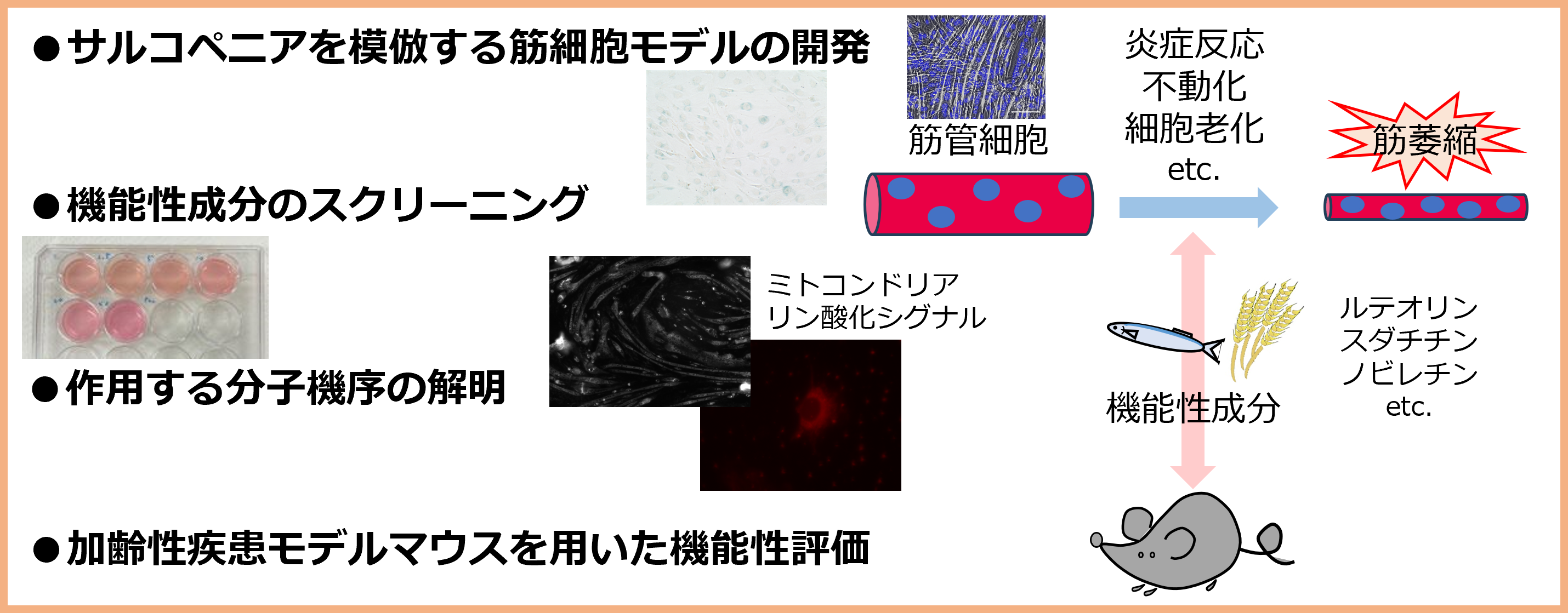
研究課題4:筋細胞を用いたモデル開発と機能性成分の探索・作用機序解明
研究担当者:安倍 知紀
骨格筋は運動器として日々の生活活動を支えるのみならず、代謝や神経活動の調節も担っています。私は、健康寿命の延伸を実現するためには、骨格筋の質・量の改善が重要な鍵を握ると考えています。加齢によるサルコペニア発症の新規分子機序の解明と、筋細胞モデルの開発から機能性成分の探索・作用機序の解明を行うことで、食による骨格筋の質・量の改善を目指します。
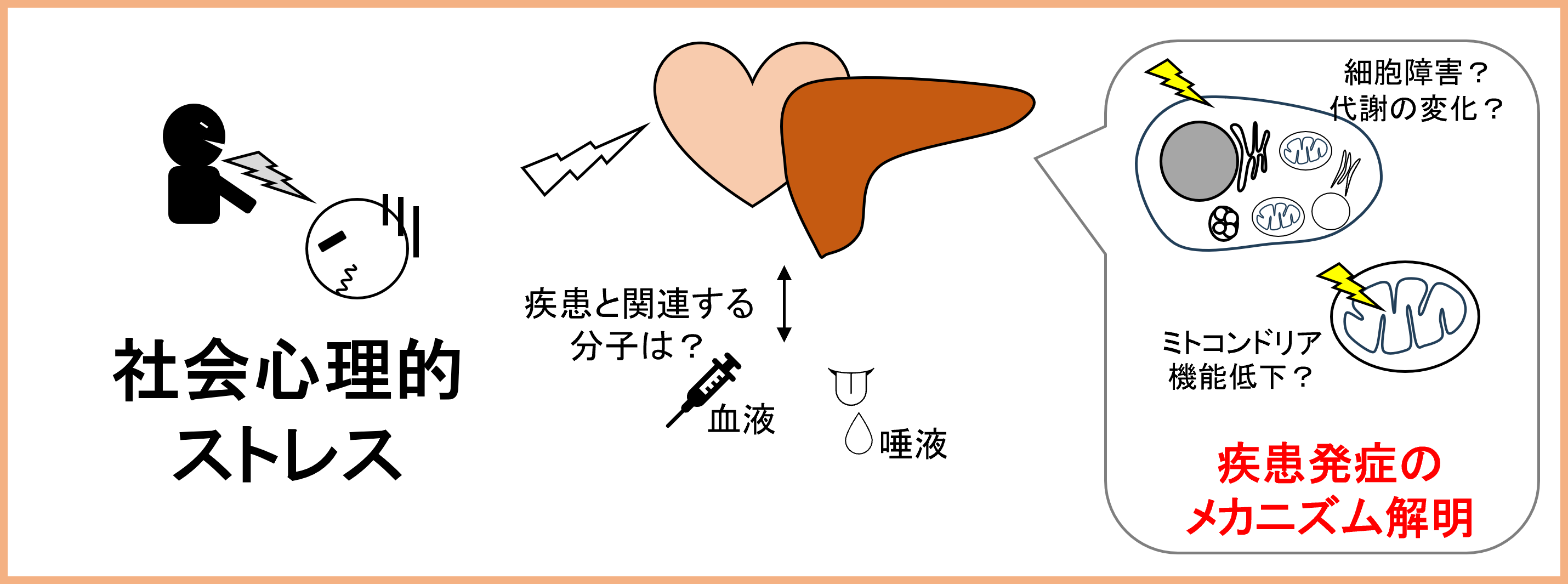
研究課題5:心理的ストレスがもたらす疾患の病態解明とその未病マーカーの開発
研究担当者:佐藤 智之
心理的ストレスは、うつ病などの精神疾患の原因となるだけでなく、肝疾患や心疾患の発症リスクを増大させることが知られています。本課題では主に社会心理的ストレスモデルマウスを用いて、心理的ストレスが肝臓や心臓にもたらす影響の解明を目指すとともに、疾患発症を予測できる未病マーカーの開発に取り組んでいます。 この他、培養細胞や単離ミトコンドリアを用いて、肝疾患や神経疾患の発症メカニズムの解明と、生活習慣による介入方法の開発にも取り組んでいます。
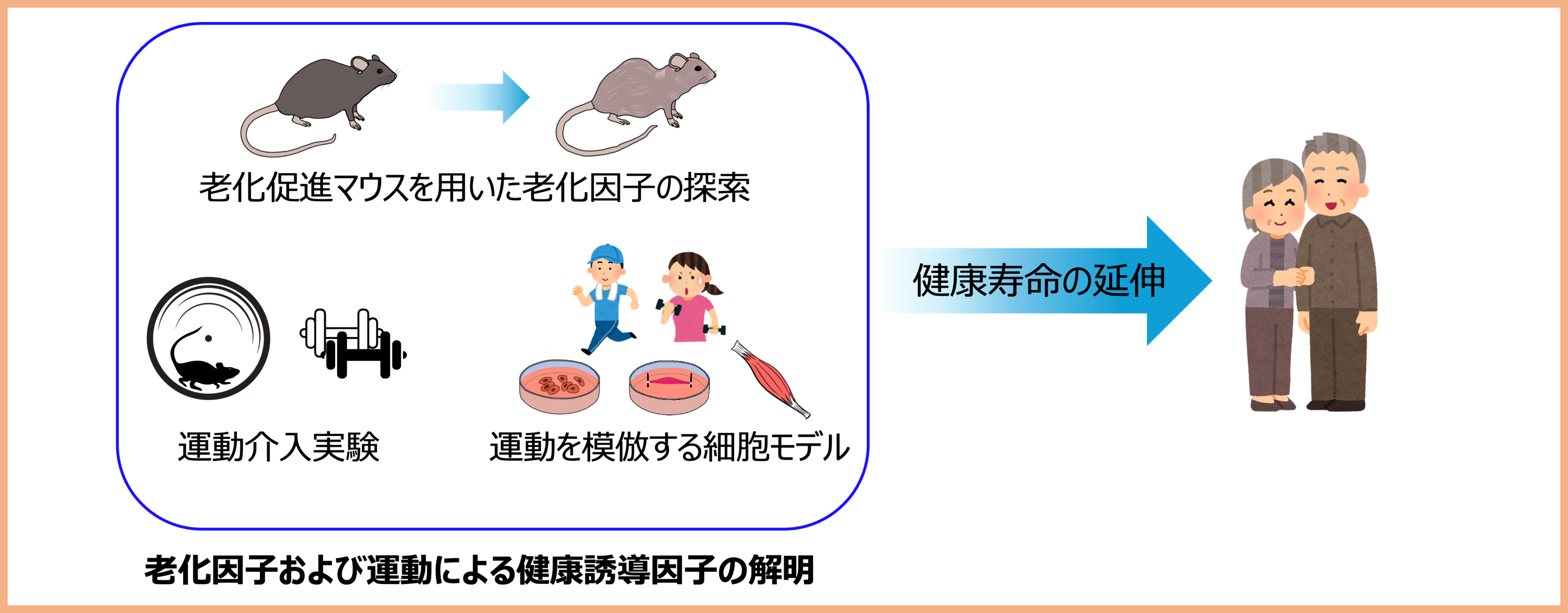
研究課題6:老化因子の探索と運動による未病改善メカニズムの解明
研究担当者:李 ミンジョン
超高齢化社会においては健康寿命の延伸が重要な課題ですが、老化によりがんや認知症など多くの疾患のリスクが高まることが知られています。そこで本研究では、老化のメカニズムを分子レベルで明らかにすることを目的とし、老化促進モデルマウスを用いて老化因子の探索を行っています。さらに、未病の段階から健康維持に寄与するとされる運動にも着目し、実験動物を用いた運動介入実験を実施しています。また、運動の生理的効果を細胞レベルで再現するための模倣技術の開発にも取り組んでいます。これらの研究を通じて、老化や未病の進行に関与する新たな分子メカニズムおよび運動による健康効果の解明を目指しています。
グループの構成メンバー
| 顔写真 | 所属・役職および名前 | 専門分野 | その他、etc |
|---|---|---|---|
 |
研究グループ長 新海 陽一 |
|
|
 |
上級主任研究員 大石 勝隆 |
|
|
 |
主任研究員 桑原 知子 |
|
|
 |
主任研究員 安倍 知紀 |
|
|
 |
主任研究員 佐藤 智之 |
|
|
 |
研究員 李 ミンジョン |
|
業績リスト
- Mishima, T; Takenaka, Y; Hashimoto-Hachiya, A; Tanigawa, Y; Suzuki, N; Oishi, K; Ogasawara, R.
Time-of-day effect of high-intensity muscle contraction on mTOR signaling and protein synthesis in mice.
SCIENTIFIC REPORTS. 2025 Jul 3;15(1):23702. doi: 10.1038/s41598-025-06709-z - Oishi, K; Yoshida, Y; Kaida, K; Terai, K; Yamamoto, H; Toyoda, A.
Potential non-invasive biomarkers of chronic sleep disorders identified by salivary metabolomic profiling among middle-aged Japanese men.
SCI REP. 2025 Apr 21;15(1):10980. doi:10.1038/s41598-025-95403-1 - Hagihara, H; Shoji, H; Hattori, S; Sala, G; Takamiya, Y; Tanaka, M; Ihara, M; Shibutani, M; Hatada, I; Hori, K;... Oishi, K; ... Miyakawa, T.
Large-scale animal model study uncovers altered brain pH and lactate levels as a transdiagnostic endophenotype of neuropsychiatric disorders involving cognitive impairment.
Elife. 2024 Mar 26:12:RP89376. doi: 10.7554/eLife.89376 - Ohkura, N; Morimoto-Kamata ,R; Kamikubo, Y; Takahashi, Y; Oishi, K.
Hypofibrinolytic phenotype in Tsumura Suzuki Obese Diabetes (TSOD) mice unrelated to hyperglycemia.
Drug Discov Ther. 2023 Nov 18;17(5):346-350. doi: 10.5582/ddt.2023.01064 - Ohkura, N; Morimoto-Kamata, R; Oishi, K; Higo-Yamamoto, S; Fujinami, A; Inoue, KI; Ohta, M.
Supplementation with Ashitaba (Angelica keiskei) yellow stem exudate prevents aging-induced thrombotic tendencies and systemic inflammation without affecting body weight gain in mice.
J Med Food. 2023 Nov;26(11):843-848. doi: 10.1089/jmf.2023.K.0140 - Oishi, K; Yajima, Y; Yoshida, Y; Hagihara, H; Miyakawa, T; Higo-Yamamoto, S; Toyoda, A.
Metabolic profiles of saliva in male mouse models of chronic sleep disorders induced by psychophysiological stress.
Sci Rep. 2023;13(1):11156. doi: 10.1038/s41598-023-38289-1 - Sato, T; Oishi, K.
Time-restricted feeding has a limited effect on hepatic lipid accumulation, inflammation and fibrosis in a choline-deficient high-fat diet-induced murine NASH model.
PLOS ONE. 2024 Jan 29;19(1):e0296950. doi: 10.1371/journal.pone.0296950 - Sato, T; Ochiishi, T; Higo-Yamamoto, S; Oishi, K.
Circadian and sleep phenotypes in a mouse model of Alzheimers disease characterized by intracellular accumulation of amyloid β oligomers.
EXP ANIM. 2023 Dec 14. doi: 10.1538/expanim.23-0104 - Zhuang, HT; Fujikura, Y, Ohkura, N; Higo-Yamamoto, S; Mishima, T; Oishi, K.
A ketogenic diet containing medium-chain triglycerides reduces REM sleep duration without significant influence on mouse circadian phenotypes.
FOOD RESEARCH INTERNATIONAL. 2023 Jul;169:112852. doi: 10.1016/j.foodres.2023.112852 - Abe, T, Sato, T, Murotomi, K.
Sudachitin and Nobiletin Stimulate Lipolysis via Activation of the cAMP/PKA/HSL Pathway in 3T3-L1 Adipocytes.
FOODS. 2023 May 10;12(10):1947. doi: 10.3390/foods12101947 - Yoshida, Y; Yajima, Y; Fujikura, Y; Zhuang, H; Higo-Yamamoto, S; Toyoda, A; Oishi, K.
Identification of salivary microRNA profiles in male mouse model of chronic sleep disorder.
Stress. 2022;26(1):21-28. doi: 10.1080/10253890.2022.2156783 - Yoshida, Y; Yajima, Y; Kawakami, K; Nakamura, S; Tsukahara, T; Oishi, K; Toyoda, A.
Salivary microRNA and metabolic profiles in a mouse model of subchronic and mild social defeat stress.
Int J Mol Sci. 2022;23:14479. doi: 10.3390/ijms232214479 - Horikawa, K; Hashimoto, C; Kikuchi, Y; Makita, M; Oishi, K.
Wheat alkylresorcinol increases fecal lipid excretion and suppresses feed efficiency in mice depending on the time of supplementation.
Nutrition. 2022;103-104:111796. doi: 10.1016/j.nut.2022.111796 - Ohkura, N; Taniguchi, M; Oishi, K; Inoue, K; Ohta, M.
Angelica keiskei (Ashitaba) has potential as an antithrombotic health food.
Food Res. 2022;6(2):18-24. doi: 10.26656/fr.2017.6(2).121 - Abe, T.
Timing of Medium-Chain Triglyceride Consumption Modulates Effects in Mice with Obesity Induced by a High-Fat High-Sucrose Diet.
NUTRIENTS. 2022 Dec 1;14(23):5096. doi: 10.3390/nu14235096 - Fujikura, Y; Yamanouchi, K; Sugihara, H; Hatakeyama, M; Abe, T; Ato, S; Oishi, K.
Ketogenic diet containing medium-chain triglyceride ameliorates transcriptome disruption in skeletal muscles of rat models of duchenne muscular dystrophy.
BIOCHEM BIOPHYS REP. 2022 Nov 11;32:101378. doi: 10.1016/j.bbrep.2022.101378 - Fujikura, Y; Kimura, K; Yamanouchi, K; Sugihara, H; Hatakeyama, M; Zhuang, H; Abe, T; Daimon, M; Morita, H; Komuro, I; Oishi, K.
A medium-chain triglyceride containing ketogenic diet exacerbates cardiomyopathy in a CRISPR/Cas9 gene-edited rat model with Duchenne muscular dystrophy.
SCI REP. 2022 Jul 8;12(1):11580. doi: 10.1038/s41598-022-15934-9 - Konishi, T; Takahashi, Y; Shiina, Y; Oike, H; Oishi, K.
Time-of-day effects of consumption of fish oil-enriched sausages on serum lipid parameters and fatty acid composition in normolipidemic adults: A randomized, double-blind, placebo-controlled, and parallel-group pilot study.
Nutrition. 2021;90:111247. doi: 10.1016/j.nut.2021.111247 - Fujikura, Y; Sugihara, H; Hatakeyama, M; Oishi, K; Yamanouchi, K.
Ketogenic diet with medium-chain triglycerides restores skeletal muscle function and pathology in a rat model of Duchenne muscular dystrophy.
FASEB J. 2021 Sep;35(9):e21861. doi: 10.1096/fj.202100629R